نشانگر مولکولی AFLP
در سال ۱۹۹۵ نشانگر مولکولی AFLP ابداع و معرفی شدند. که به نظر می رسید بسیاری از محدودیت های نشانگرهای پیشین را نداشته باشند. با روش AFLP نشانگرهایی تولید می شوند که علاوه بر دارا بودن مزایای RFLP مانند دقت و تکرارپذیری، ویژگی های مثبت روش های مبتنی بر واکنش زنجیره ای پلیمراز را نیز دارند. پایه این روش تکثیر انتخابی برخی قطعه ها از بین تمام قطعه های هضم شده DNA است.
با استفاده از این روش، تعداد زیادی از قطعه های حاصل از هضم، تکثیر و قابل رویت می شوند. این در حالی است که نیازی به دانش اولیه در مورد ردیف بازی قطعه هایی که تکثیر می شوند، وجود ندارد. هر یک از این قطعه ها می توانند به عنوان یک نشانگر ژنتیک مورد استفاده قرار گیرند. تعداد قطعه هایی که با این روش تکثیر می شوند، به دقت و توانمندی روش های جداسازی توسط الکتروفورز و تعداد نوکلئوتید اضافه شده به انتهای آغازگر بستگی دارد. معمولا در این روش بین ۵۰ تا ۱۰۰ قطعه حاصل از هضم تکثیر و با استفاده از ژل های پلی اکریل امید واسرشته ساز ثبت می شوند.

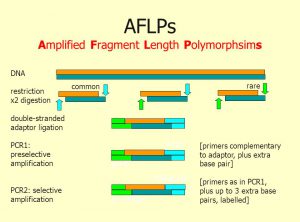
روش نشانگر مولکولی AFLP سه مرحله مجزا دارد
۱ – هضم DNA را با یک جفت آنزیم محدودگر و دوخت آنها به آداپتورهای الیگونوکلئوتیدی
۲ – طراحی، ساخت آغازگر و تکثیر انتخابی دسته ای از قطعه های حاصل از هضم: با استفاده از ردیف بازی آداپتورهایی که معلوم است و نیز ردیف بازی نقاط برش، طراحی و ساخت آغازگر انجام می شود. اما برای تکثیر انتخابی قطعه های حاصل از هضم دو، سه یا چند نوکلئوتید به انتهای ‘۳ ردیف آغازگر اضافه می شود. در نتیجه فقط قطعه هایی تکثیر شوند که ردیف بلافصل آنها در مجاورت نقطه برش، مکمل نوکلئوتیدهای یاد شده باشد.
۳- جداسازی قطعه های حاصل از تکثیر بر روی ژل های ردیف یابی پلی اکریلامید
۴- خود پرتونگاری یا رنگ آمیزی نقره برای ثبت نتیجه ها.
تفاوت و تنوع مشاهده شده به وسیله این نشانگر به صورت حضور یا عدم حضور باند و به دلایل زیر است
الف – اختلاف در جایگاه های برشی
ب – کمبود یا اضافه شدن نوکلئوتید در داخل قطعه های برشی
ج – بروز پدیده حذف و اضافه در محل اتصال آغازگر یا درون قطعه قابل تکثیر
مزایای نشانگرهای مولکولی AFLP
- این روش در مقایسه با سایر روش ها بیشترین تعداد نشانگرها به ازای هر ژل را ایجاد می کند.
- این روش واجد کلیه مزایای روش RAPD از جمله سرعت و عدم نیاز به اطلاعات اولیه در مورد ردیف بازی DNA و غیره است.
- در این روش نیازی به تهیه و تدارک و نگهداری کاوشگر نیست.
- دقت و تکرارپذیری این نشانگر بدلیل انتخاب دمای زیاد هم رشته سازی و اتصال آغازگر به DNA الگو بیشتر از RAPD است. اگرچه موضوع عدم تکرارپذیری یکی از دغدغه های کاربران این نشانگر است.
- فراوانی بسیار زیاد این نشانگرها که از طریق تنظیم تعداد و نوع نوکلئوتیدهای اضافی در انتهای ‘۳ و تغییر آنزیم محدودگر تحصیل می شود
معایب نشانگرهای AFLP
۱- پیچیدگی نسبی این روش در مقایسه با سایر روش های مبتنی بر PCR
۲- عدم اطلاع از جایگاه ژنی نشانگرها
۳- غالب بودن این نشانگرها موجب عدم امکان تشخیص افراد خالص از ناخالص می گردد. بسیاری از تفاوت های مشاهده شده بر روی ژل هایی که تعداد زیادی باند تولید می کنند، به طور ذاتی از نوع غالب و مغلوب نیستند. به عبارت دیگر بیشتر آنها از نوع همبارز هستند. به دلیل اینکه تشخیص سیستم اللى در آنها مشکل است، از نظر کاربردی و تجزیه و تحلیل، ناگریز به تلقی آنها به عنوان نشانگرهای غالب خواهیم بود.
۴- عدم امکان تشخیص الل های هر نشانگر موجب افت کارایی این نشانگر می شود
۵- تکثیر قطعه های غیر واقعی در AFLP موجب کاهش قابلیت اعتماد این روش می گردد. از این رو باید مطمئن باشیم که برش کامل DNA صورت گرفته است. به منظور برش کامل DNA باید از نمونه با کیفیت مطلوب و مقدار مناسب آنزیم های محدودگر استفاده کرد.
همچنین آنزیم های محدودگر حساس به متیل گذاری موجب عدم برش کامل DNA را می شوند. با افزایش درجه حرارت مرحله اتصال و استفاده از آغازگرهای طویل تر، می توان قطعه های غیر واقعی ایجاد شده را به کمترین حد ممکن کاهش داد. از طرف دیگر سختی زیاد شرایط PCR موجب می شود که آغازگر به طور کامل به DNA الگو بچسبد. در نتیجه مانع جفت شدن ناقص آغازگر و تشکیل باندهای ناخواسته شود.
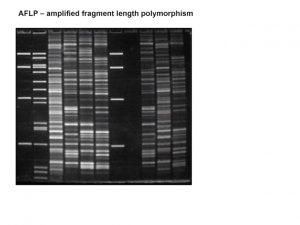
منبع: کتاب نشانگرهای مولکولی، انتشارات دانشگاه تهران.










دیدگاهتان را بنویسید